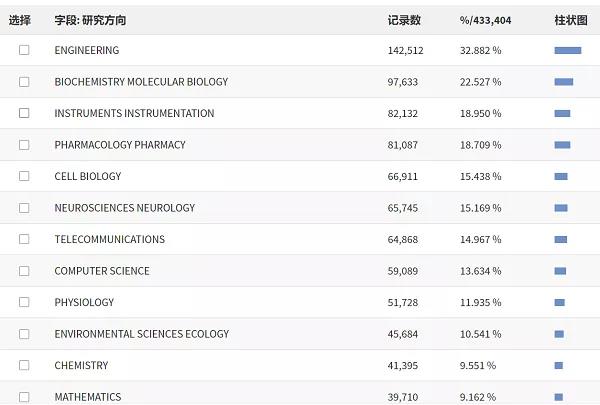
皮膚是人體(tǐ)最大(dà)、最易接觸的器官。通過納米微針打開(kāi)皮膚管道,隻需要一(yī)張貼片透皮給藥,不僅可以減輕病人痛苦,還有減少毒副作用等優點,同時貼片也被做成生(shēng)物(wù)傳感器等用于實時監測,因此貼片(patch)受到廣大(dà)研究人員(yuán)的關注。通過Web of Science(SCI)檢索關于貼片(patch)研究的發文情況,截止2021年5月19日,如圖1所示其主要研究方向是生(shēng)物(wù)醫學領域,其中(zhōng)在化學和材料科學領域發表的文章分(fēn)别達到了41395篇和39710篇。因此,本次選擇了近期在Nature/Science子刊上發表的關于貼片的部分(fēn)成果,對它們進行簡要的介紹,供大(dà)家了解和學習!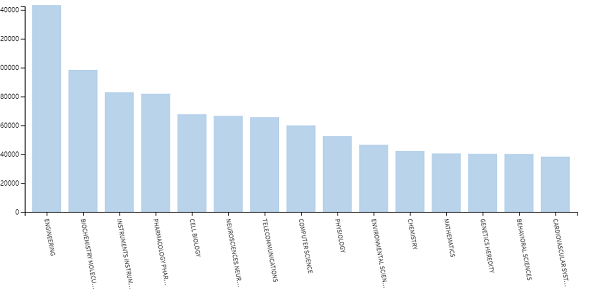

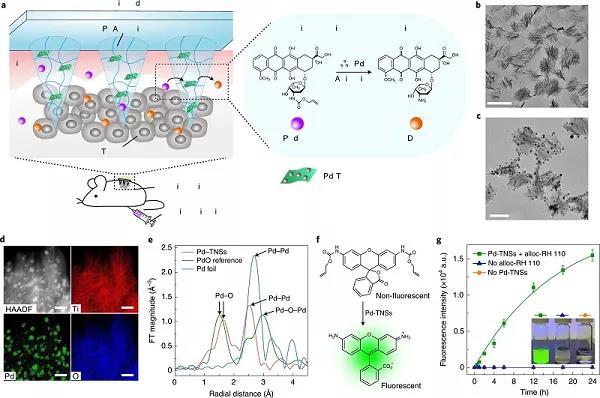
過渡金屬介導的生(shēng)物(wù)正交催化激發了人工(gōng)化學的一(yī)個新分(fēn)支,與酶促反應互補,使生(shēng)物(wù)分(fēn)子的選擇性标記或通過非自然過程原位合成生(shēng)物(wù)活性劑成爲可能。然而,由于金屬毒性的安全問題和催化劑的應用過程複雜(zá)等原因,生(shēng)物(wù)正交催化在體(tǐ)内的有效應用仍然具有挑戰性。基于此,浙江大(dà)學顧臻教授(通訊作者)等人報道了一(yī)種具有生(shēng)物(wù)正交催化活性的微針陣列貼片裝置。作者以聚乙烯醇(PVA)爲基體(tǐ),沉積有钯納米粒子(Pd NPs)的TiO2納米片(Pd-TNSs)爲納米填料,制備了該微針陣列貼片裝置。其中(zhōng),摻入Pd-TNSs可以增強微針在幹玻璃狀态下(xià)的力學性能,賦予它們足夠的強度,以微創的方式穿透皮膚。當置于水環境中(zhōng)時,微針就會變成膨脹的水凝膠狀态,形成多孔結構。因此,三個層次的結構層次,即三維(3D)針陣列、每個針基質中(zhōng)的微孔和網絡中(zhōng)高度暴露的Pd-TNSs表面,促進了籠狀分(fēn)子的擴散以與Pd納米粒子接觸,從而促進了它們的活化。需注意,通過使用小(xiǎo)鼠黑色素瘤模型,證明了系統給藥的前藥N-烯丙基氧羰基籠狀阿黴素(alloc-DOX)的局部腫瘤内活化,不僅能夠增加劑量,而且限制了對健康器官和組織的副作用。此外(wài),Pd-TNSs與PVA之間的界面相互作用以及PVA鏈形成的氫鍵使得微針針尖在水合物(wù)狀态下(xià)具有足夠的力學韌性,從而易于去(qù)除整個貼片,而不會留下(xià)有害的過渡金屬(TMs)或引起炎症。

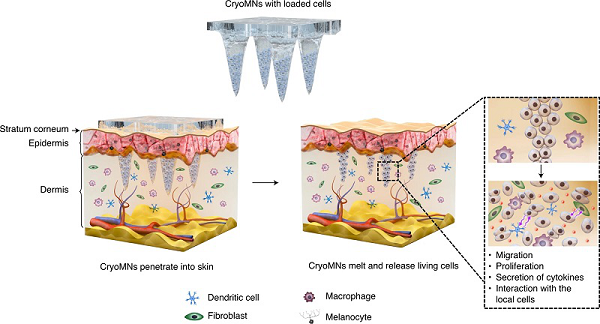
研究發現,簡單、安全和有效的治療細胞的透皮遞送技術有助于治療皮膚疾病的細胞療法。通過皮下(xià)注射針頭的常規細胞遞送與患者依從性差有關,存在需要經過培訓的人員(yuán)、産生(shēng)廢物(wù)且具有不可忽視的傷害和感染風險的問題。基于此,香港城市大(dà)學Chenjie Xu(通訊作者)等人報道了一(yī)種冷凍微針貼片的設計和概念應用,并且該冷凍微針貼片可用于活細胞的透皮傳遞。這種微針是用預先懸浮的細胞在低溫培養基中(zhōng)進行分(fēn)步低溫微模塑法制備而成,在細胞複蘇後可以很容易插入豬皮中(zhōng)溶解。在小(xiǎo)鼠體(tǐ)内,冷凍微針遞送的細胞保留了它們的生(shēng)存能力和增殖能力。在患有皮下(xià)黑色素瘤的小(xiǎo)鼠中(zhōng),通過冷凍微針遞送的卵清蛋白(bái)脈沖的樹(shù)突狀細胞引起了更高的抗原特異性免疫反應,并且導緻腫瘤生(shēng)長比靜脈和皮下(xià)注射的細胞更慢(màn)。具有生(shēng)物(wù)相容性的冷凍微針可促進微創細胞遞送,用于一(yī)系列的細胞治療。

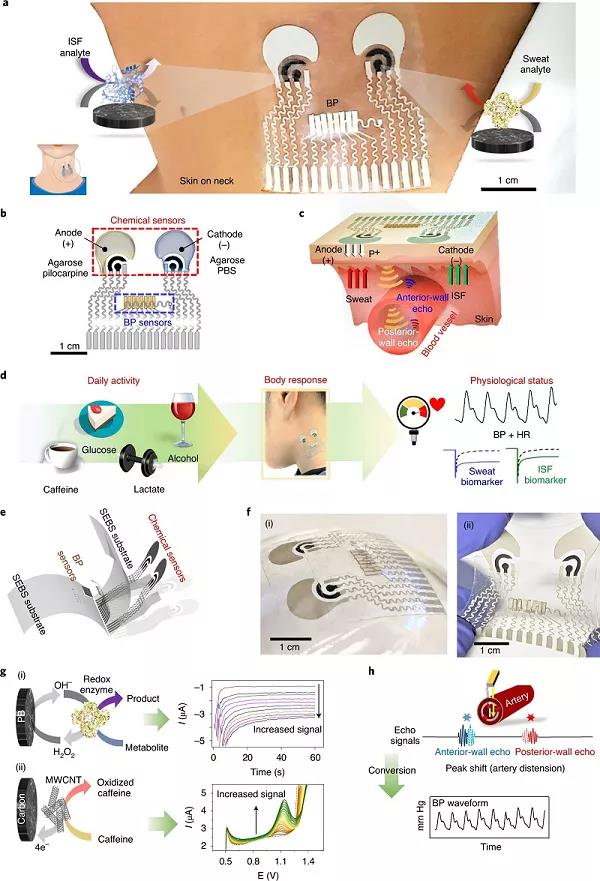
爲了監測日常活動對人體(tǐ)生(shēng)理反應的影響,需要一(yī)種能夠同時跟蹤代謝和血流動力學參數的可穿戴器件。基于此,美國加州大(dà)學聖地亞哥分(fēn)校Joseph Wang和Sheng Xu(共同通訊作者)等人報道了一(yī)種非侵入性皮膚穿戴器件,通過超聲波傳感器同時監測血壓和心率,并通過電(diàn)化學傳感器同時監測多種生(shēng)物(wù)标志(zhì)物(wù)。作者優化了集成器件,使其在符合彎曲皮膚表面的同時提供力學彈性和靈活性,并且确保可靠地感知(zhī)組織間液中(zhōng)的葡萄糖和汗液中(zhōng)的乳酸、咖啡因和酒精,而各個傳感器之間沒有串擾。在人類志(zhì)願者身上,該器件捕捉到了食物(wù)攝入和運動的生(shēng)理效應,特别是在食物(wù)消化後葡萄糖的産生(shēng),通過糖酵解消耗葡萄糖,以及血壓和心率的增加,以補償氧氣的消耗和乳酸的産生(shēng)。通過集成的可穿戴器件進行連續、同步的聲學和電(diàn)化學傳感,可以豐富對人體(tǐ)日常活動響應的理解,并且有助于對異常生(shēng)理變化的早期預測。

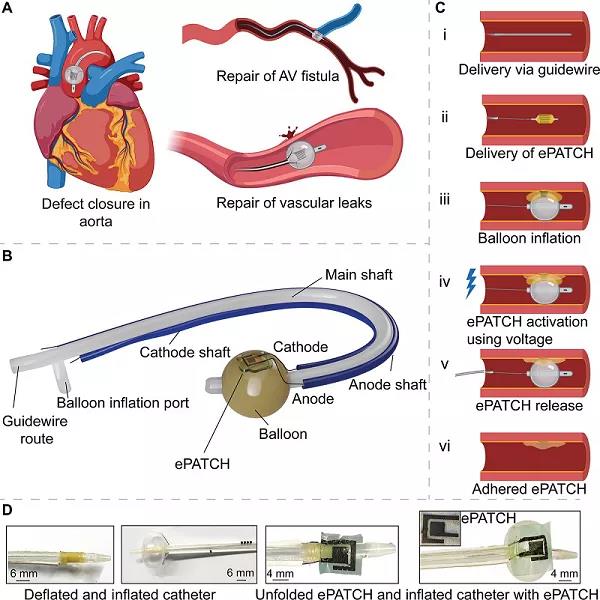
腔内缺損的外(wài)科手術修複與圍手術期發病率和死亡率有關。利用組織粘合劑進行血管内修複可以減少宿主組織損傷,但是目前的生(shēng)物(wù)粘合劑設計不支持微創部署。其中(zhōng),電(diàn)壓激活的組織粘合劑爲腔内修複提供了一(yī)種新的策略。爲了促進電(diàn)壓激活粘合劑的臨床轉化,新加坡南(nán)洋理工(gōng)大(dà)學Terry W. J. Steele和麻省理工(gōng)學院Ellen T. Roche(共同通訊作者)等人報道了将一(yī)種電(diàn)壓激活貼片(ePATCH)與一(yī)種帶有可拉伸電(diàn)極的微創導管(CATRE)配對,以對抗體(tǐ)内和體(tǐ)外(wài)管腔缺陷的修複。ePATCH/CATRE平台展示了在濕組織基底上密封直徑高達2 mm的管腔缺損。防水密封件具有柔韌性和回彈力,可承受20000多次生(shēng)理相關的應力/應變循環。當心髒跳動時,ePATCH被電(diàn)激活,沒有觀察到電(diàn)信号中(zhōng)斷。ePATCH/CATRE平台具有廣泛的潛在應用,從假性動脈瘤/瘘的血管内治療到生(shēng)物(wù)電(diàn)極,再到電(diàn)生(shēng)理标測。

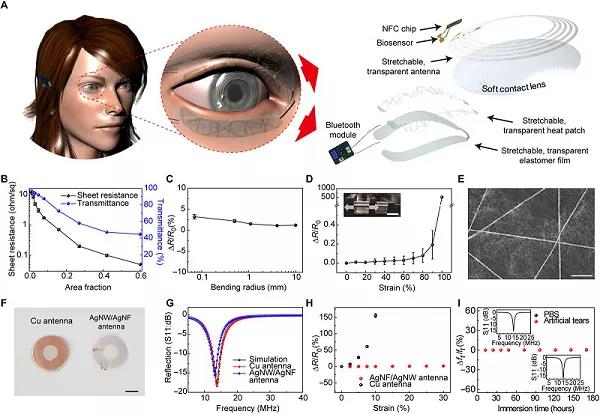
可穿戴電(diàn)子器件能夠監測人體(tǐ)的生(shēng)理信号,提供生(shēng)物(wù)醫學信息,已成爲可持續的個人健康管理領域的熱點。基于此,韓國延世大(dà)學Jang-Ung Park和韓國慶北(běi)大(dà)學Hong Kyun Kim(共同通訊作者)等人報道了一(yī)種用于無線監測和治療慢(màn)性眼表炎症(OSI)的柔性、智能隐形眼鏡和可連接皮膚的治療器件的人類先導性實驗。作爲一(yī)種診斷器件,這種智能隐形眼鏡能夠使用石墨烯場效應晶體(tǐ)管實時測量淚液中(zhōng)基質金屬蛋白(bái)酶-9(OSI的生(shēng)物(wù)标志(zhì)物(wù))的濃度。作爲一(yī)種治療器件,作者還制備了一(yī)種可拉伸、透明的貼片,可以貼附在人眼睑上。其中(zhōng)診斷和治療器件都可以使用智能手機進行無線通信,從而實現OSI的實時診斷和自動熱療。此外(wài),作者利用活體(tǐ)動物(wù)和人體(tǐ)進行的體(tǐ)内實驗證實,作爲一(yī)種無創、可移動的保健解決方案,它們具有良好的生(shēng)物(wù)相容性和可靠性。

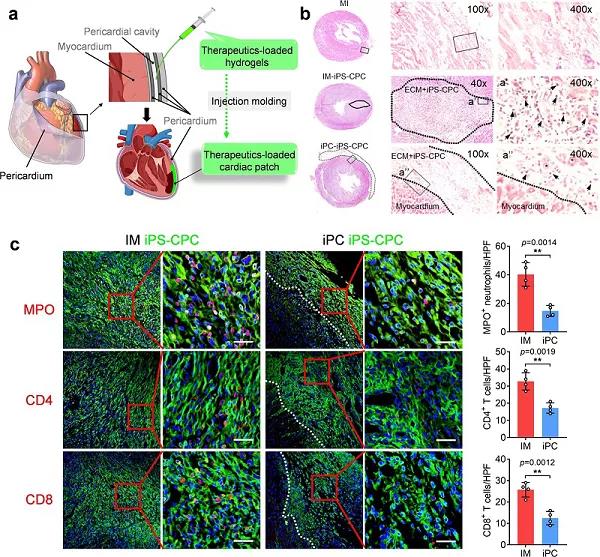
心髒貼片是一(yī)種向心髒遞送治療藥物(wù)的有效方法。然而,這種手術通常是侵入性且很難進行的。基于此,美國北(běi)卡羅萊納州立大(dà)學Ke Cheng(通訊作者)等人開(kāi)發并測試一(yī)種方法,利用心包腔作爲一(yī)個自然模型,在心包内注射生(shēng)物(wù)相容性水凝膠中(zhōng)的治療藥物(wù)後原位形成心髒貼片。在齧齒類動物(wù)心肌梗死模型中(zhōng),作者證明了心包内注射是一(yī)種有效且安全的方法來遞送含有誘導多能幹細胞衍生(shēng)的心髒前體(tǐ)細胞或間充質幹細胞來源的外(wài)泌體(tǐ)的水凝膠。在注射後,水凝膠在心包腔形成心髒貼片狀結構,減輕免疫反應,增加治療藥物(wù)的心髒滞留時間。通過強大(dà)的心血管修複和心外(wài)膜源性細胞的刺激,遞送的治療減輕心髒重構和改善心肌梗死後心髒功能。此外(wài),作者在臨床相關的豬模型上證明了微創心包内注射的可行性。總之,該研究證實了心包内注射是一(yī)種安全有效的方法,可以将治療性水凝膠遞送到心髒進行心髒修複。

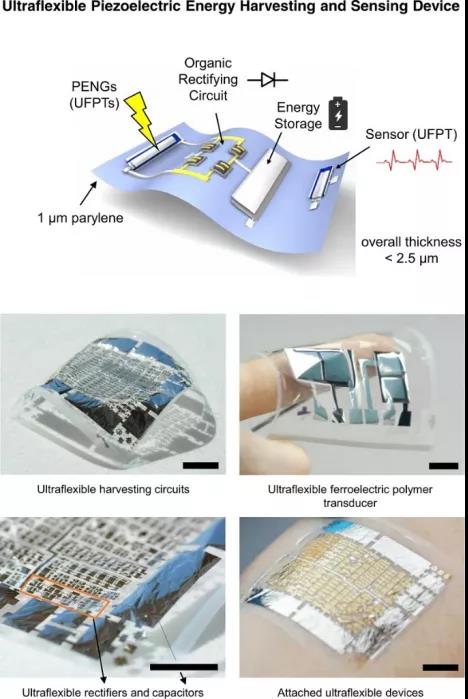
能源自主性和整合性是下(xià)一(yī)代可穿戴和柔性電(diàn)子産品的基本要素,用于醫療保健、機器人和信息物(wù)理系統。基于此,日本大(dà)阪大(dà)學Tsuyoshi Sekitani和奧地利Barbara Stadlober(共同通訊作者)等人首次報道了一(yī)種由壓電(diàn)納米發電(diàn)機、二極管整流器和儲能電(diàn)容組成的綜合性超柔性能量收集器件(UEHD),所有組件的厚度均不超過2.5 µm,在僅1 μm的聚對二甲苯制成的薄基闆上制成。當附着在人體(tǐ)皮膚的表面上時難以察覺,作者展示了一(yī)種鐵電(diàn)無線電(diàn)子保健貼片,可以監測脈搏率并測量血壓。納米發電(diàn)機和傳感器都是基于P(VDF:TrFE)70:30的超柔性鐵電(diàn)聚合物(wù)傳感器(UFPTs)。同時,結合了由有機二極管制成的超柔性全波整流器電(diàn)路,具有短OTFT幾何形狀和超柔性薄膜電(diàn)容器使用納米氧化鋁薄層。作者采用DNTT(二萘并噻吩)作爲有機半導體(tǐ)的二極管顯示出很高的整流比,超過107,并且由于它們的過電(diàn)壓低于100 mV,因此内置的電(diàn)壓降可忽略不計。其中(zhōng),UFPTs具有以下(xià)優點:(1)超柔韌性,使其能夠共形附着于各種材料和表面,并允許将多層UFPTs堆疊在3D形狀的載體(tǐ)上;(2)對平面外(wài)(橫向)應力的高靈敏度,可通過多層堆疊提高,從而實現預彎曲橡膠載體(tǐ)上三層堆疊的峰值靈敏度在15 nC N-1範圍内;(3)極好的機械穩定性,允許在40 µm彎曲半徑下(xià)穩定運行;(4)響應時間非常短,遠低于20 ms N-1。此外(wài),UFPTs用作脈沖電(diàn)源時,峰值功率密度超過3 mW cm-3。

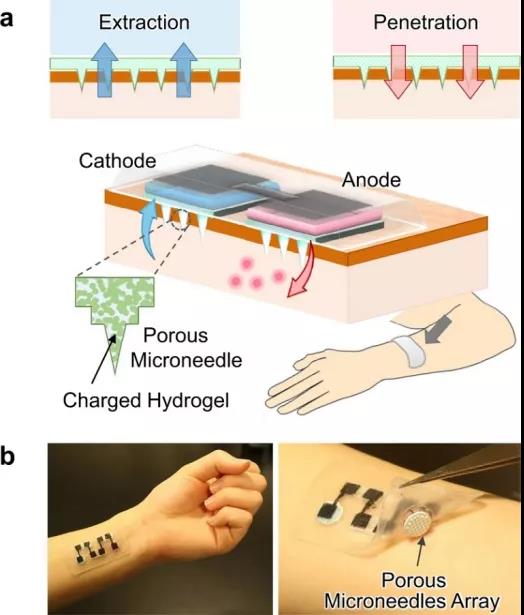
微針陣列是一(yī)種具有吸引力的選擇,通過微創手段來突破皮膚屏障進行有效的透皮給藥。基于此,日本東北(běi)大(dà)學Matsuhiko Nishizawa(通訊作者)等人報道了一(yī)種基于固體(tǐ)聚合物(wù)的離(lí)子導電(diàn)多孔微針(PMN)貼片,其可應用于改善離(lí)子透入方面,是一(yī)種通過皮膚的直流電(diàn)增強透皮分(fēn)子傳輸的技術。利用帶電(diàn)水凝膠修飾的PMN在離(lí)子電(diàn)滲療法中(zhōng)有以下(xià)三個創新優勢:(1)通過低侵入性穿刺高阻力角質層來降低透皮阻力;(2)通過相互連接的微孔輸送大(dà)分(fēn)子;(3)産生(shēng)電(diàn)滲流(EOF)。特别是,PMN産生(shēng)的EOF極大(dà)地提高了透皮分(fēn)子的滲透或提取,類似于由外(wài)部壓力引起的流動。作者利用豬皮樣品證明了EOF輔助遞送模型藥物(wù)(右旋糖酐)和葡萄糖提取的提高效率。此外(wài),通過内置的酶生(shēng)物(wù)電(diàn)池(果糖/O2電(diàn)池)爲基于PMN的透皮EOF系統供電(diàn)也被證明是一(yī)種可能的全有機離(lí)子導入貼片。

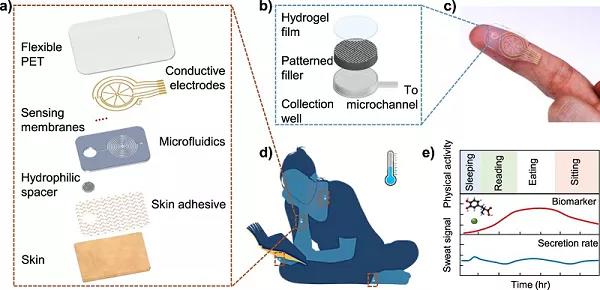
在久坐和日常活動中(zhōng),人體(tǐ)自然持續地分(fēn)泌汗液進行體(tǐ)溫調節,其速率可以反映潛在的健康狀況,包括神經損傷、自主神經和代謝紊亂以及慢(màn)性應激。然而,低分(fēn)泌率和蒸發對收集靜止的體(tǐ)溫調節汗液進行無創的身體(tǐ)生(shēng)理學分(fēn)析提出了挑戰。基于此,美國加州大(dà)學伯克利分(fēn)校Ali Javey(通訊作者)等人報道了一(yī)種可穿戴式的貼片,将其用于在休息時連續監測汗液,使用微流控技術來防止蒸發,并且實現對分(fēn)泌速率的選擇性監測。作者将用于快速吸汗的親水性填充物(wù)集成到傳感通道中(zhōng),減少了實時測量所需的汗液累積時間。此外(wài),作者還集成了用于pH、Cl-和左旋多巴監測的電(diàn)化學傳感器。作者還展示了與日常活動、應激事件、低血糖引起的出汗和帕金森(sēn)病相關的動态出汗分(fēn)析的貼片功能。通過支持與久坐、常規和日常活動兼容的汗液分(fēn)析,這些貼片可以在休息時對身體(tǐ)生(shēng)理進行連續、自主的監測。
文章轉載自微信公衆号:材料人